Внутренняя энергия
Из курса физики VII класса известно, что любое макроскопическое тело обладает внутренней энергией.
Понятие внутренней энергии макроскопических тел играет важнейшую роль при исследовании тепловых явлений. Это обусловлено существованием фундаментального закона природы — Закона сохранения энергии.
Открытие закона сохранения энергии стало возможным после того, как было доказано, что наряду с механической энергией микроскопические тело обладают еще и внутренней энергией, заключенной внутри самих тел. Эта энергия входит в общий баланс
Когда скользящая по льду шайба останавливается под действием силы трения, то ее механическая (кинетическая) энергия не просто исчезает, а передается хаотически движущимся молекулам льда и шайбы. Неровности поверхностей трущихся тел деформируются при движении, и интенсивность хаотического движения молекул возрастает. Оба тела нагреваются, что и означает увеличение их внутренней энергии.
Нетрудно наблюдать обратный переход внутренней энергии в механическую. Если нагревать воду в пробирке, закрытой пробкой, то внутренняя энергия воды начнет возрастать. Вода закипит и давление пара увеличится настолько, что пробка будет выбита и полетит вверх. Кинетическая энергия пробки увеличивается за счет внутренней энергии пара. Расширяясь, водяной пар совершает работу и охлаждается.
Его внутренняя энергия при этом уменьшается.
С точки зрения молекулярно-кинетической теории внутренняя энергия макроскопического тела равна сумме кинетических энергий хаотического движения всех молекул (или атомов) относительно центра масс тела и потенциальных энергий взаимодействия всех молекул друг с другом (но не с молекулами других тел). Вычислить внутреннюю энергию тела (или ее изменение), учитывая движение отдельных молекул и их положения друг относительно друга, практически невозможно из-за огромного числа молекул в макроскопических телах. Необходимо поэтому уметь определять внутреннюю энергию (или ее изменение) в зависимости от макроскопических параметров, которые можно непосредственно измерять.
Внутренняя энергия идеального одноатомного газа. Наиболее прост по своим свойствам одноатомный газ, состоящий из отдельных атомов, а не молекул. Одноатомными являются инертные газы — гелий, неон, аргон и др.
Вычислим внутреннюю энергию идеального одноатомного газа.
Так как молекулы идеального газа не взаимодействуют друг с другом, за исключением коротких интервалов времени, когда они сталкиваются, их потенциальная энергия считается равной нулю. Вся внутренняя энергия идеального газа представляет собой кинетическую энергию теплового движения его молекул.
Для вычисления внутренней энергии идеального одноатомного газа массы M нужно умножить среднюю энергию (2.9) одного атома на число атомов.
Это число равно произведению количества вещества 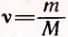 на постоянную Авогадро NA (см. § 2, формулы 1.3 и 1.7).
на постоянную Авогадро NA (см. § 2, формулы 1.3 и 1.7).
Умножая (2.9) на 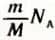 , получим внутреннюю энергию идеального одноатомного газа:
, получим внутреннюю энергию идеального одноатомного газа: 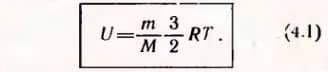 Внутренняя энергия идеального одноатомного газа прямо пропорциональна его абсолютной температуре.
Внутренняя энергия идеального одноатомного газа прямо пропорциональна его абсолютной температуре.
Если идеальный газ состоит из более сложных молекул, чем одноатомный, то его внутренняя энергия также пропорциональна абсолютной температуре, но коэффициент пропорциональности между U и T другой. Объясняется это тем, что сложные молекулы не только движутся поступательно, но и вращаются. Внутренняя энергия таких газов равна сумме энергий поступательного и вращательного движения молекул.
Зависимость внутренней энергии от макроскопических параметров. Мы установили, что внутренняя энергия идеального газа зависит от одного параметра температуры. От объема внутренняя энергия идеального газа не зависит потому, что потенциальная энергия взаимодействия его молекул считается равной нулю.
У реальных газов, жидкостей и твердых тел средняя потенциальная энергия взаимодействия молекул не равна нулю. Правда, для газов она много меньше средней кинетической энергии, но для твердых и жидких тел сравнима с кинетической. Средняя потенциальная энергия взаимодействия молекул зависит от объема вещества, так как при изменении объема меняется среднее расстояние между молекулами.
Следовательно, Внутренняя энергия в общем случае наряду с температурой T зависит еще и от объема V.
Так как значения макроскопических параметров T, V и других однозначно определяют состояние тел, то, следовательно, они определяют и внутреннюю энергию макроскопических тел.
Внутренняя энергия U макроскопических тел однозначно определяется параметрами, характеризующими состояние тел:
U = U(T, V).
Для идеального одноатомного газа это уравнение принимает форму (4.1).
Теперь рассмотрим, в результате каких процессов может меняться внутренняя энергия. Из курса физики VII класса известно, что существует два рода таких процессов совершение работы и передача теплоты. Вначале более детально, чем в VII классе, рассмотрим работу в термодинамике.
