Первый закон термодинамики
Закон сохранения энергии. К середине XIX в. многочисленные опыты ученых доказали, что механическая энергия никогда не пропадает бесследно. Опускаются гири, вращающие лопасти в сосуде с ртутью, и температура ртути повышается на строго определенное число градусов.
Падает молот на кусок свинца, и свинец нагревается тоже вполне определенным образом.
На основании множества подобных наблюдений и обобщения опытных фактов был сформулирован Закон сохранения энергии:
Энергия в природе не возникает из ничего в не исчезает: количество
Закон сохранения энергии управляет всеми явлениями природы и связывает их воедино. Он выполняется абсолютно точно: не известно ни одного случая, когда бы этот закон не выполнялся.
Этот закон был открыт а середине XIX в. немецким ученым, врачом по образованию, Р. Майером (1814-1878), английским ученым Д. Джоулем (1818-1889) и получил наиболее полную формулировку в трудах немецкого ученого Г. Гельмгольца (1821-1894).
Первый закон термодинамики. Закон сохранения и превращения энергии, распространенный на тепловые явления, носит название первого закона термодинамики.
В термодинамике рассматриваются тела, положение центра тяжести которых практически не изменяется. Механическая энергия тел остается постоянной, изменяться может лишь внутренняя энергия.
До сих пор мы рассматривали процессы, в которых внутренняя энергия системы менялась либо за счет совершения работы, либо за счет теплообмена с окружающими телами. В общем случае при переходе системы из одного состояния в другое внутренняя энергия будет меняться одновременно как за счет совершения работы, так и за счет передачи теплоты. Первый закон термодинамики формулируется именно для таких общих случаев:
Изменение внутренней энергии системы при переходе ее из одного состояния в другое равно сумме работы внешних сил и количества теплоты, переданного системе:
ΔU = A + Q (4.10)
Первый закон термодинамики (4.10) связывает изменение внутренней энергии с изменением макроскопических параметров V и T, так как через изменения этих параметров выражается работа и количество теплоты.
В частном случае изолированной системы над ней не совершается работа (A = 0), и она не обменивается теплотой с окружающими телами (Q = 0). Согласно первому закону термодинамики в этом случае ΔU = U2 — U1 = 0, или U1 = U2. Внутренняя энергия изолированной системы остается неизменной (сохраняется).
Часто вместо работы A внешних тел над системой рассматривают работу A’ системы над внешними телами. Учитывая, что A’ = — A (см. §16), первый закон термодинамики (4.10) можно записать так:
Q = ΔU + A’ (4.11)
Количество теплоты, переданное системе, идет на изменение ее внутренней энергии и на совершение системой работы над внешними телами.
Невозможность создания вечного двигателя. Из первого закона термодинамики вытекает невозможность создания вечного двигателя — устройства, способного совершать неограниченное количество работы без затрат топлива или каких-либо других материалов. Если к системе не поступает теплота (Q = 0), то работа A’ согласно (4.11) может быть совершена только за счет убыли внутренней энергии: A’ = — ΔU.
После того как запас энергии окажется исчерпанным, двигатель перестанет работать.
Работа и количество теплоты — характеристики процесса изменения энергии. В данном состоянии система всегда обладает определенной внутренней энергией. Но нельзя говорить, что в ней содержится определенное количество теплоты или работы.
Как работа, так и количество теплоты являются величинами, характеризующими изменение энергии системы в результате того или иного процесса.
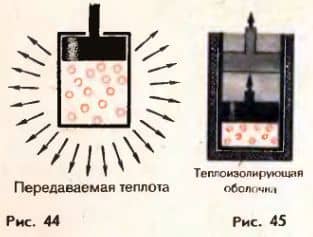
Внутренняя энергия системы может измениться одинаково как за счет совершения системой работы, так и за счет передачи окружающим телам какого-то количества теплоты. Нагретый газ в цилиндре может уменьшить свою энергию. остывая, без совершения работы (рис. 44). Но он может потерять точно такое же количество энергии, перемещая поршень, без отдачи теплоты окружающим телам. Для этого стенки цилиндра и поршень должны быть теплонепроницаемыми (рис.
45).
В дальнейшем на протяжении всего курса физики мы будем знакомиться с различными другими формами энергии, способами их превращения и передачи.