Строение вещества
1. Основные положения молекулярно-кинетической теории
Напомним известные вам из курса физики основной школы сведения о строении вещества.
Атомная гипотеза
Мысль о том, что вещество состоит из мельчайших частиц, высказал еще древнегреческий философ Демокрит. Греки придумали и название для этих частиц — атомы. (Атом в переводе с греческого означает «неделимый». Но в 20-и веке ученые смогли «разделить» не только атом, но даже атомное ядро.) Но гениальная гипотеза Демокрита ждала опытных подтверждений больше двух тысяч
Расскажем о некоторых из них.
Броуновское движение. В начале 19-го века английский ботаник Роберт Броун, наблюдая в микроскоп крошечные частицы пыльцы, находящиеся в воде, обнаружил, что они пребывают в «вечной пляске».
Хаотичность движения броуновских частиц иллюстрирует рисунок 38.1. Отрезками соединены последовательные положения броуновской частицы через каждые 30 с. 
В конце 19-го века ученые догадались, что броуновское движение обусловлено бомбардировкой крошечных частиц движущимися молекулами жидкости. Дело в том, что частицы размером в несколько микронов «чувствуют» удары молекул, подобно тому как маленькие лодочки качаются даже на невысокой волне. (Микрон — одна тысячная доля миллиметра.)
? 1. Почему броуновское движение не прекращается?
Теорию броуновского движения построили крупнейший физик 20-го века Альберт Эйнштейн (жил и работал в Швейцарии, Германии и США) и польский физик Мариан Смолуховский. Из их расчетов следовало, что размер молекулы воды меньше одной миллионной доли миллиметра. Поэтому молекулы невозможно увидеть даже в самый лучший оптический микроскоп.
Но ученые все-таки смогли их увидеть!
Миллионную долю миллиметра (10-9 м) называют нанометром. От слова «нанометр» произошло название нанотехнологии — чрезвычайно перспективной области современных исследований, в которой изучают и даже проектируют объекты атомных размеров.
Развитие нанотехнологии приводит к революции в средствах связи, компьютерах, робототехнике, медицине и т. д. Ученые приступили даже к созданию нанороботов, то есть роботов, размеры которых сопоставимы с размерами молекул.
Броуновское движение стало одним из первых опытных подтверждений существования и движения молекул. Расскажем еще об одном опытном подтверждении этих фактов.
Диффузия
Поставим опыт Нальем в высокий стеклянный сосуд голубой раствор медного купороса, а поверх него, очень осторожно, — чистую воду (рис. 38.2, а). Резкая граница раздела жидкостей постепенно начнет размываться (рис.
38.2, б). Через некоторое время окраска жидкости станет однородной (рис. 38.2, в).
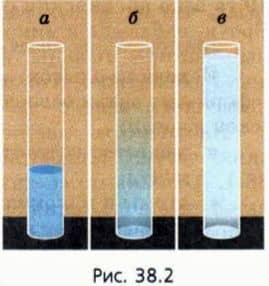 Это означает, что частицы, из которых состоят молекулы медного купороса (положительно и отрицательно заряженные ионы), проникают в воду, а молекулы воды — в медный купорос.
Это означает, что частицы, из которых состоят молекулы медного купороса (положительно и отрицательно заряженные ионы), проникают в воду, а молекулы воды — в медный купорос.
Взаимное проникновение частиц одного вещества между частицами другого, обусловленное их движением, называют диффузией (от латинского «диффузио» — распространение, растекание). Она происходит в газах, жидкостях и даже твердых телах.
Диффузия также является опытным подтверждением существования и движения молекул.
Взаимодействие молекул
Поставим опыт Плотно прижмем один к другому ; хорошо зачищенные торцы двух свинцовых цилиндров (рис. 38.3). Вследствие действия сил межмолекулярного притяжения цилиндры «сцепляются» так, что к ним можно подвесить гирю. 
Исследования показывают, что молекулы притягиваются на больших (по сравнению с размерами молекул) расстояниях, а на малых расстояниях молекулы отталкиваются. (Взаимодействие молекул описывается с помощью квантовой механики — науки о движении и взаимодействии мельчайших частиц вещества. Об основных ее положениях мы расскажем в курсе физики 11-го класса.)
Благодаря притяжению молекул, существуют жидкости и твердые тела. Они почти несжимаемы — это подтверждает, что на малых расстояниях молекулы отталкиваются.
Три положении молекулярно-кинетической теории
Исходя из опытов, в 18-19 веках ученые различных стран сформулировали основные положения молекулярно-кинетической теории:
- Вещество состоит из атомов и молекул; Атомы и молекулы находятся в непрерывном хаотическом движении; Атомы и молекулы взаимодействуют друг с другом.
Основоположники молекулярно-кинетической теории — русский ученый Михаил Васильевич Ломоносов, английские ученые Джон Дальтон и Джеймс Максвелл, немецкий ученый Рудольф Клаузиус и австрийский ученый Людвиг Вольцман. 
Фотографии атомов
В 20-м веке ученые изобрели микроскопы, позволяющие получить изображения атомов. (Речь идет об электронном и ионном микроскопах. Ион — атом или молекула, образующаяся в результате потери или присоединения одного или нескольких электронов.) На рисунке 38.4 приведена фотография поверхности золотой фольги при;увеличении в 20 миллионов раз. 
? 2. Используя эту фотографию, оцените: а) размер одного атома золота; б) каким стал бы ваш рост, если бы вы увеличились тоже в 20 миллионов раз. Сравните его с диаметром Земли.
2. Основная задача молекулярно-кинетической теории
Макроскопические и микроскопические параметры
(Названия этих слов происходят от греческих слов «макро»- большой и «микро» — малый.)
Макроскопические параметры характеризуют состояние тел в целом, а микроскопические — свойства молекул.
Макроскопические параметры: масса образца, объем образца, давление, температура.
Микроскопические параметры: масса молекулы, число молекул в образце, средняя скорость молекул, средняя кинетическая энергия молекул.
Основная задача молекулярно-кинетической теории состоит в том, чтобы найти соотношения между макроскопическими и микроскопическими параметрами и объяснить свойства вещества, исходя из представлений о движении и взаимодействии частиц вещества (атомов и молекул).
Для газов это сделали в 19-м веке, построив кинетическую теорию газов. А вот строение жидкостей и твердых тел ученые смогли понять только в 20-м веке с появлением квантовой механики.
3. Агрегатные состояния вещества
Из курса физики основной школы вы уже знаете, что большинство окружающих нас тел находятся в одном из трех агрегатных состояний. Это твердые тела, жидкости и газы. Твердые тела бывают кристаллическими и аморфными. (От греческого «аморфос» — не имеющий формы.)
В кристаллах атомы или молекулы расположены упорядоченно, образуя кристаллическую решетку. Примеры: поваренная соль, сахар, металлы.
На рисунке 38.5 схематически изображена кристаллическая решетка поваренной соли (NaCl). Кристаллические тела плавятся при определенной температуре, характерной для данного вещества. 
В аморфных телах и жидкостях молекулы расположены тоже вплотную, но порядка в их расположении нет. Примеры: смола и стекло.
На рисунке 38.6 схематически изображена молекулярная структура аморфных тел и жидкостей. У аморфных тел нет определенной температуры плавления: они размягчаются постепенно. 
Расстояния между молекулами газов намного превышают размеры самих молекул (рис. 38.7).
Например, в окружающем воздухе расстояние между молекулами примерно в 10 раз больше размеров молекул, из которых состоит воздух (в основном это двухатомные молекулы азота и кислорода). 
Состояние того или иного вещества определяется тем, насколько сильно взаимодействуют его атомы или молекулы друг с другом, а также температурой и давлением.
Атомы и молекулы веществ, которые мы считаем»твердыми», взаимодействуют настолько сильно, что при комнатной температуре это взаимодействие удерживает атомы в узлах кристаллической решетки. (При этом они совершают хаотические колебания, обусловленные тепловым движением.) Поэтому железо, например, находится в кристаллическом состоянии. При нагревании кинетическая энергия хаотического движения атомов увеличивается, и при 1539 ºС это движение разрушает кристаллическую структуру: железо плавится. При дальнейшем нагревании энергия хаотического движения атомов становится настолько большой, что связи между ними разрываются, и при 3200 ºС железо становится газом.
А вот молекулы веществ, которые мы привычно считаем газами, взаимодействуют друг с другом слабее. Энергии их хаотического движения даже при комнатной температуре хватает на то, чтобы разрывать связи между молекулами. Поэтому, например, водород при комнатной температуре является газом. Но если понизить температуру до -253 ºС, то кинетическая энергия хаотического движения молекул уменьшится настолько, что вследствие даже слабого взаимодействия они начнут «прилипать» друг к другу при столкновениях.
Водород станет превращаться в жидкость, При дальнейшем охлаждении роль взаимодействия молекул будет становиться все больше, и при -259 ºС образуется кристаллический водород.
? 3. Может ли одно и то же вещество находиться одновременно в трех разных состояниях? Приведите примеры, подтверждающие ваш ответ. Почему свойства всех газов очень похожи, а свойства жидкостей и твердых тел различны?
Опыты показывают, что свойства различных газов очень сходны (ниже мы рассмотрим это подробно). А вот твердые тела и жидкости сильно разнятся по своим свойствам.
Объясняется это тем, что молекулы газов взаимодействуют только при сравнительно редких столкновениях. Поэтому свойства газов определяются в основном движением молекул. А оно во всех газах одинаково: между столкновениями молекулы движутся равномерно и прямолинейно. (Молекулы, состоящие из двух или большего числа атомов, могут еще вращаться и совершать колебания.
Это приводит к некоторым отличиям в свойствах газов.) Свойства же твердых тел и жидкостей определяются в основном взаимодействием атомов и молекул. А поскольку атомы и молекулы различных веществ взаимодействуют по-разному, то и свойства жидкостей и твердых тел чрезвычайно разнообразны.
4. Температура и ее измерение
Тепловое равновесие и температура
Если холодное и горячее тела соприкасаются, то холодное тело будет нагреваться, а горячее — остывать. Температуры тел будут изменяться, пока не станут равными. Итак, основное свойство температуры состоит в том, что
Тела, находящиеся в тепловом равновесии, имеют одинаковую температуру.
Измерение температуры
Для измерения температуры используют термометры. Всем знакомы жидкостные термометры (рис. 38.8), действие которых основано на том, что жидкости при нагревании расширяются.  Шкала Цельсия. (Эта температурная шкала названа по имени шведского ученого, предложившего ее прообраз.) В этой наиболее распространенной у нас шкале температуру таяния льда принимают за 0 градусов, а температуру кипения воды при атмосферном давлении — за 100 градусов.
Шкала Цельсия. (Эта температурная шкала названа по имени шведского ученого, предложившего ее прообраз.) В этой наиболее распространенной у нас шкале температуру таяния льда принимают за 0 градусов, а температуру кипения воды при атмосферном давлении — за 100 градусов.
Температуру по шкале Цельсия записывают, используя маленькую букву t — например, так: t = 20 ºС.
Какой жидкостный термометр показывает температуру правильно? Если бы мы захотели при изготовлении жидкостного термометра разделить шкалу между 0 ºС и 100 ºС на равные части, то показания наших самодельных термометров при промежуточных температурах зависели бы от того, каную жидкость мы взяли. Например, когда столбик ртутного термометра достиг бы 50-го деления, глицериновый не добрался бы до 48-го, потому что ртуть и глицерин расширяются по-разному.
Какой же из этих термометров считать правильным?
К счастью, выяснилось, что все газы при нагревании расширяются практически одинаково. Поэтому газовые термометры намного более точные. Свойства газов мы рассмотрим в следующих параграфах подробнее.

Дополнительные вопросы и задания
4. Капелька оливкового масла объемом 1 мм3 растекается по площади не более 1 м2. Оцените размер молекулы масла.
5. Какой длины получилась бы цепочка из молекул воды, содержащейся в одной чайной ложке (5 мл), если бы эти молекулы выстроились в одну линию? Для оценки можно заменить молекулу кубом с длиной ребра 0,3 нм. Сравните получившуюся величину с расстоянием от Земли до Солнца (150 миллионов километров).
6. Объясните, почему броуновское движение можно наблюдать только для достаточно малых частиц.
7. Можно ли считать беспорядочное движение пылинок в воздухе броуновским движением?
8. Почему молекулы, из которых состоит воздух, не падают на поверхность Земли подобно каплям дождя?
9. Запах вещества переносят его молекулы. При комнатной температуре молекулы движутся со скоростями в сотни метров в секунду. Почему же тогда запах пролитых духов достигает другого конца комнаты только через несколько секунд?
10. Какая общая особенность движения молекул и планет делает возможным их непрекращающееся движение?
11. Что общего у диффузии и броуновского движения и чем они отличаются друг от друга?
12. Найдите связи между следующими макроскопическими и микроскопическими параметрами: а) массой образца вещества m, массой одной молекулы m0 и числом молекул в образце N; б) объемом образца вещества V; числом молекул в образце N и размером одной молекулы d. При расчете примите, что молекула занимает объем куба с длиной ребра d.
13. Исходя из известных вам представлений о строении вещества, выскажите предположение: где скорость диффузии наибольшая — в газах, жидкостях или твердых телах? Где наименьшая? Обоснуйте свое предположение.

